ELEKTRON İLGİSİ Nedir? Elektron İlgisi Sıralaması Soruları Grup Sıralaması
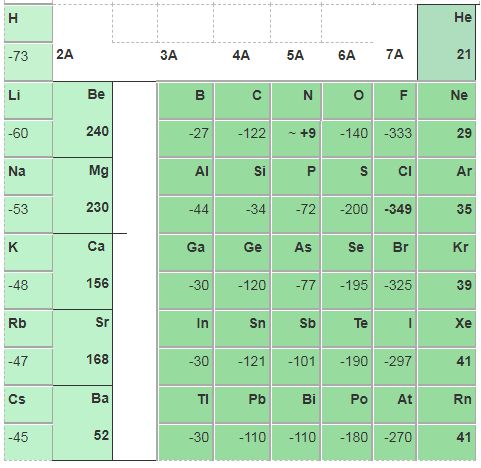
ELEKTRON İLGİSİ Nedir? Elektron İlgisi Sıralaması Soruları Grup Sıralaması Elektron İlgisi Nedir? Tanımı Elektron ilgisi, gaz hâldeki bir atomun bir elektron alması sırasında oluşan enerji değişimidir. Elektron ilgisi, bir elementlerin elektron almaya ya da almamaya olan eğilimlerinin ölçüsüdür.Birimi genelde kJ/mol KiloJoule/mol) cinsindendir. F (g) + e– → F–(g+ 78,4 kkal Eİ=- 78,4 kkal Cl(g)) + e– → Cl–(g) +… Daha fazlasını oku »ELEKTRON İLGİSİ Nedir? Elektron İlgisi Sıralaması Soruları Grup Sıralaması