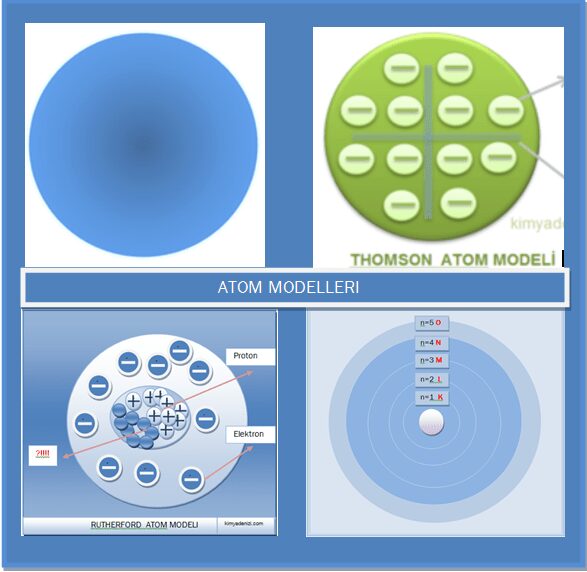
Protonun Keşfi Protonun Keşfine Katkı Sağlamış Bilim Adamları
Proton keşfinde bir çok bilim adamının katkıları olmasına rağmen bazı bilim adamları biraz daha öne çıkmaktadır.Bunlardan bazıları;
William Prout Protonun Keşfine Katkıları (1815)
Protonla ilgili ilk ciddi çalışmalar aynı anda doktor olan İngiliz kimyacı ve fizyolojist William Prout tarafından
1815 yılında ortaya kondu, Tüm atomların ”protyles” olarak adlandırdığı hidrojen atomlarından oluştuğunu söylüyordu.
William Prout; o sırada mevcut olan atom ağırlıklarının tablolarına dayanarak, her elementin atom ağırlığının, hidrojen atomunun tamsayısı katsayıları olduğunu iddia ederek, hidrojen atomunun tek gerçek temel parçacık olduğunu öne sürdü. ve diğer elementlerin atomları çeşitli sayılarda hidrojen atomlarından oluşan gruplardan oluşur.
Prout hipotezi daha sonra protonu keşfeden Ernest Rutherford’un protonu keşfetmesinde temel bir bakış açısı olmuştur.
Antonius Van Den Broek Protonun Keşfine Katkıları (1911)
Periyodik tablodaki yerinin atom numarasının atom çekirdeğinin yüküne karşılık geldiğini ilk fark eden Hollandalı amatör bir fizikçiydi.
Bu hipotez 1911’de yayımlandı ve 1913’te deneysel kanıtlar bulan Henry Moseley’in deneysel çalışmasına ilham verdi.
Henry MOSELEY in ”Atomun temel kimliğini proton sayıları belirler”görüşünün temellerini atan aslında amatör bir fizikçi olan Van Den Broek tur
Eugen Goldstain Protonun Keşfine Katkıları
1886 da yaptığı çalışmalarda Crooks tüplerinde pozitif yüklü taneciklerin de ışıma yaptığını farketti Crooks tüpleri ile deney yaptığı sıralarda katot ışınları oluşurken meydana gelen pozitif iyonların da ışıma yaptığını gözlemledi…
– Delikli bir katot levha kullanarak deneyi tekrarladı. Pozitif yüklü ışınlar katotun deliklerinden geçerek doğrusal ışın oluşturdu. Pozitif iyonların oluşturduğu bu ışınlara pozitif ışınlar veya kanal ışınları adı verilir.
– Katot ışınları tüp içinde yol alırken, çarptıkları atom ya da moleküllerden elektron koparırlar ve + yük oluştururlar . Elektron kopmasıyla oluşan bu pozitif iyonlar, katot yönüne geçerler.
– Kanallar sayesinde görülebildiği için bu ışınlar “Kanal Işınları” ya da “Pozitif Işınlar” olarak adlandırılırlar
– Bu ışınlar ilk olarak Eugen Goldstein tarafından 1886’da araştırılmıştır.
– 1898 de Alman fizikçi W. Wien, kanal ışınlarının pozitif elektrik yüklü olduğunu gördü.
– Kanal ışınlarının “yük/ kütle” oranını kabaca hesapladı. Bu oran tüpteki gazın cinsine göre değişiyordu. Bunun sebebi; tüpte bulunan gazın cinsine göre farklı iyonların oluşmasıydı.
Wilhelm Wien ve J. J. Thomson
1898 yılında pozitif ışınların elektrik ve manyetik alanda sapmalarını inceleyerek proton için e/m değerin hesapladılar.Thomson burada da elektron için yaptıkları yöntemleri benzer bir şekilde kullandı Pozitif ışınlarla ilgili bu çalışmaları 1906 yılında Thomson açıkladı.
– Pozitif ışınların e/m değerinin maddenin türüne bağlı olduğu belirlendi.
– Sadece 1 pozitif yük bulundurmasından dolayı nedeniyle hidrojen iyonu kullanıldı
– hidrojen iyonu için bulunan e/m daha doğrusu p/m değeri 1 pozitif yüklü taneciğe yani protona ait değer olarak alındı.
– En küçük kütleli H2 gazı konulduğunda p/m değeri 9.5791.104 C/g olan pozitif yüklü taneciklerin oluştuğu görüldü.
– Elektronunu kaybetmiş olan bu en küçük hidrojen taneciğine “proton” adı verildi.
– Protonun yükü elektronun yükü ile eşit ama zıt işaretlidir.
1 protonun yükü ; +1,6022×10-19 C olarak hesaplandı.

– Bir protonun kütlesi, bir elektronun kütlesinin yaklaşık 1840 katı dır
– Bir protonun kütlesi mp=1,6726.10-24gr dır

Eugen Goldstain Protonun Keşfine Katkıları
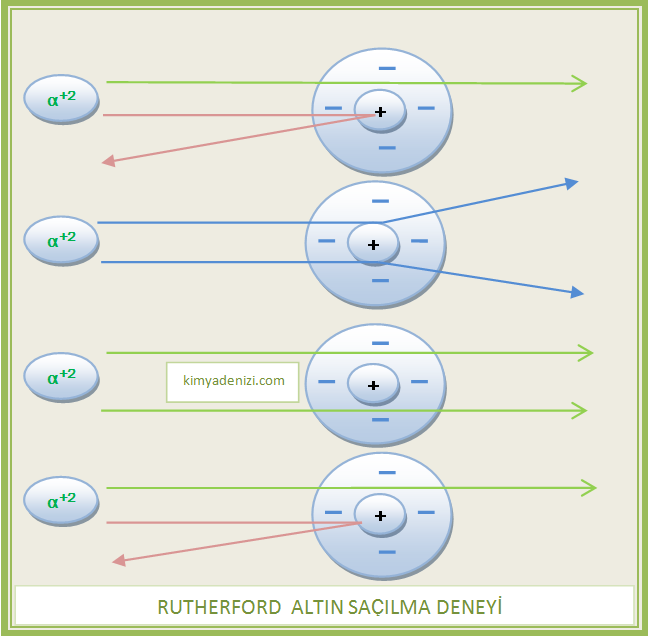
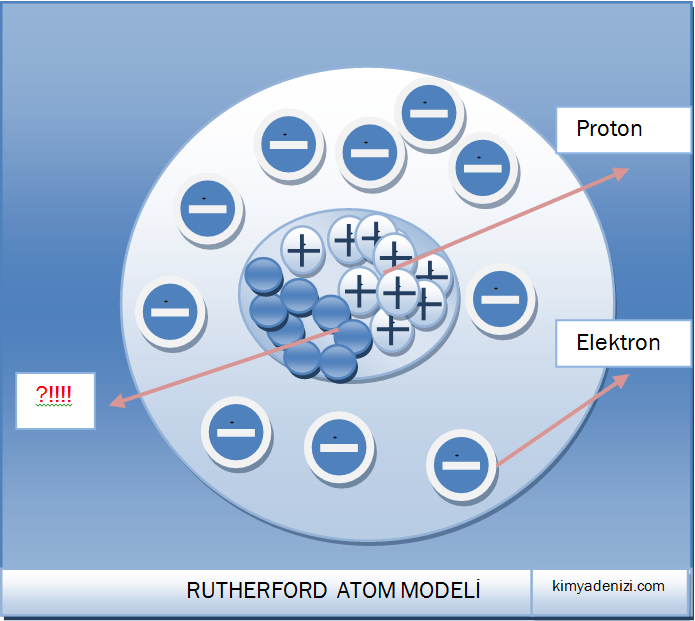
Yaptığı Altın saçılma deneyleri sonucunda 1911’de kendi adı ile anılan bir atom modeli geliştirdi.Bu modelde protonla + yüklü taneciklerle ilgili olarak aşağıdaki varsayımları öne sürdü;
– Atomda pozitif yükün tümü, küçük ama ağır kütleli Çekirdek denilen küçük bölgede toplanmıştır.
– Elektronlar, atom içinde yaklaşık olarak 10-8 cm çapında bir hacmi kapladığı hâlde, pozitif elektrik çok küçük olmakla birlikte ağır bir çekirdek içinde toplanmıştır (10-13 cm) .
– Çekirdek, elektronların yüklerini dengeleyecek kadar pozitif yük taşımaktadır.
– Atomlar nötr olduğundan , elektronlar pozitif yüklere eşit sayıdadır.
– Pozitif yüklerin toplam kütlesi atomun kütlesinin yaklaşık yarısı kadardır.
Henry G. J. Moseley Protonun Keşfine Katkıları
1913-1914 yıllar ında Henry G. J. Moseley X-ışınlarını kullanarak farklı elementlerin farklı X-ışınları spektrumunu inceledi
– 1912’de her elementin farklı karakteristik X-ışınları spektrumu verdiğini ve elementin atom kütlesi arttıkça yayınlanan ışının frekanslarının buna paralel olarak arttığını gözlemledi.
– Moseley, X-ışınları frekanslarının atomun çekirdeğindeki yükün karakteristiği olduğunu farketi.
– Moseley atomda bir elementten diğerine gidildikçe artan şeyin artı yüklü çekirdeğin yükü olabileceğini belirtti.
– Atom numarasının atom çekirdeğinde bulunan artı birimlerin sayısı olduğunu söyledi.
– Periyodik yasayı, “Elementlerin fiziksel ve kimyasal özellikleri atom numarasının periyodik işlevidir.”
şeklinde tekrar tanımlayarak bir elementi diğerinden ayıran şeyin proton sayısı olduğunu söyledi.