İyonik Bağlar Lewis gösterimi İyonik bağlı Bileşikler Lewis gösterimi
İyonik Bağlar Metaller ile ametaller arasında elektron alışverişi ile oluşan bağlardır
Metal atomları ile ametal atomları arasında itme-çekme kuvvetleri ile yani elektrostatik çekim kuvvetleri ile ile oluşan bağlar İyonik bağlar olarak adlandırılır.
Metaller fazla olan elektronlarını elektron ihtiyacı olan ametallere vererek iyonik bağ oluştuturlar.
Örnek:
NaCl iyonik bileşiğinde iyonik bağı inceleyelim
11Na atomu ile 17Cl atomu arasındaki iyonik bileşiği ve lewis yapısını inceleyelim.
11 Na11 atomu soygaz düzenine geçmek için 1 e- verir ve +1 yüklü olur
11 Na11:2.8.1 → 11 Na10+1: 2.8
17 Cl17:2.8.7 → 17 Cl18-1: 2.8.8
17Cl17 atomu soygaz düzenine geçmek için 1 e- alır ve -1 yüklü olur
Na+1 ile Cl-1 çaprazlanırsa NaCl bileşiği elde edilir
Na+1 x Cl-1→NaCl
NaCl bileşiği Lewis Simgesi Gösterimi ve İyonik Bağ oluşumu
11Na=2.8.1 Des:1 1 Nokta1 e alırNa+
17Cl =2.8.7 Des:7 7 Nokta 1 e alır Cl –
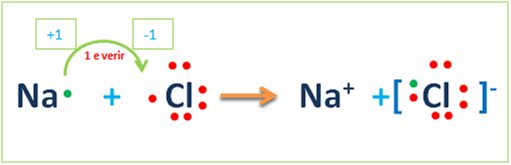
Na atomu 1 e verir +1 yüklü olur
Cl atomu 1 e alır -1 yüklü olur
 İyonik Bağlar Lewis Gösterimi İyonik Bileşiklerin Özellikleri VİDEO İZLE Youtube Kimya Denizi
İyonik Bağlar Lewis Gösterimi İyonik Bileşiklerin Özellikleri VİDEO İZLE Youtube Kimya Denizi
Örnek:
KF iyonik bileşiğinde iyonik bağı inceleyelim
19 K atomu ile 9F atomu arasındaki iyonik bileşiği inceleyelim.
19K atomu soygaz düzenine geçmek için 1 e- verir ve +1 yüklü olur
19 K19:2.8.8.1 → 19 K18+1: 2.8.8
9F9:2.7 → 9 F10-1: 2..8
9F9 atomu soygaz düzenine geçmek için 1 e- alır ve -1 yüklü olur
K+1 ile F-1 çaprazlanırsa KFbileşiği elde edilir
K+1 x F-1→KF
KF bileşiği Lewis Simgesi Gösterimi ve İyonik Bağ oluşumu
19 K=2.8.8.1 Des:1 1 Nokta 1 e alır K+
9F =2.7 Des:7 7 Nokta 1 e alır F–

K atomu 1 e verir +1 yüklü olur
F atomu 1 e alır -1 yüklü olur
Örnek:
MgCl2 iyonik bileşiğinde iyonik bağı inceleyelim
12 Mg atomu ile 17Cl atomu arasındaki iyonik bileşiği inceleyelim.
12 Mg atomu soygaz düzenine geçmek için 2e- verir ve +2 yüklü olur
12 Mg 12:2.8.2 → 12 Mg 10+22 .8
17Cl17:2.8.7 → 17Cl18:1: 2.8.8
17Cl17 atomu soygaz düzenine geçmek için 1 e- alır ve -1 yüklü olur
Mg +2ile Cl-1 çaprazlanırsa MgCl2bileşiği elde edilir
Mg+2x Cl-1→MgCl2
MgCl2bileşiği Lewis Simgesi Gösterimi ve İyonik Bağ oluşumu
12Mg2.8.2 Des:22 Nokta 1 e alır Mg+2
17Cl =2.8.7 Des:7 7 Nokta 1 e alır Cl –
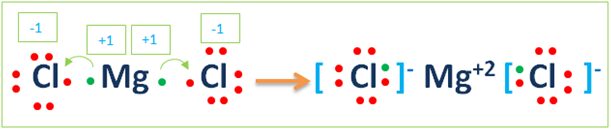
Aşağıdaki gösterim de yanlış değildir.Bazen böyle de gösterilebilir.

Mgatomu 1.e- nu verir Mg+1 olur
Mg atomu 2.e- nu verir Mg +2 olur
Cl atomları 1 e alırlar -1 yüklü olurlar
Örnek:
CaF2iyonik bileşiğinde iyonik bağı inceleyelim
20Caatomu ile 9Fatomu arasındaki iyonik bileşiği inceleyelim.
20Ca atomu soygaz düzenine geçmek için 2e- verir ve +2 yüklü olur
20Ca20:2.8.8.2 → 20 Ca18+2:2.8.8
9F9:2.7 → 9 F10-1: 2.8
9F atomu soygaz düzenine geçmek için 1 e- alır ve -1 yüklü olur
Ca+2 ile Cl-1 çaprazlanırsa CaF2 bileşiği elde edilir
Ca+2 x F-1→ CaF2
CaF2 bileşiği Lewis Simgesi Gösterimi ve İyonik Bağ oluşumu
20Ca:2.8.8.2 Des:22 Nokta 2 e alır Ca+2
9F9:2.7 Des:7 7 Nokta 1 e alır F –
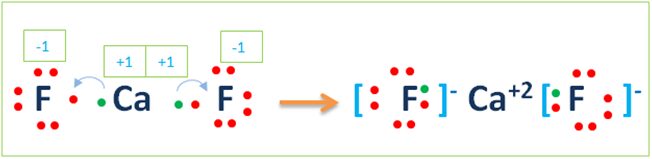
Aşağıdaki gösterim de yanlış değildir.Bazen böyle de gösterilebilir.

Ca atomu 1.e- nu verir Ca+1 olur
Ca atomu 2.e- nu verir Ca+2 olur
F atomları 1 e alırlar -1 yüklü olurlar
 9.SINIF KİMYA KAZANIM TESTLERİ ÇÖZÜMLERİ İÇİN TIKLA
9.SINIF KİMYA KAZANIM TESTLERİ ÇÖZÜMLERİ İÇİN TIKLA
Örnek:
AlCl3 iyonik bileşiğinde iyonik bağı inceleyelim
13Al atomu ile 17Cl atomu arasındaki iyonik bileşiği inceleyelim.
19Al atomu soygaz düzenine geçmek için 3e- verir ve +3 yüklü olur
13Al13:2.8.3 → 13Al10+22 .8
17Cl17:2.8.7 → 17Cl18:1: 2.8.8
17Cl17atomu soygaz düzenine geçmek için 1 e- alır ve -1 yüklü olur
Al+3ile Cl-1 çaprazlanırsa AlCl3 bileşiği elde edilir
Al+3x Cl-1→ AlCl3
AlCl3bileşiği Lewis Simgesi Gösterimi ve İyonik Bağ oluşumu
13Al:2.8.3 Des:33 Nokta 1 e alır Al+3
17Cl =2.8.7 Des:7 7 Nokta 1 e alır Cl –
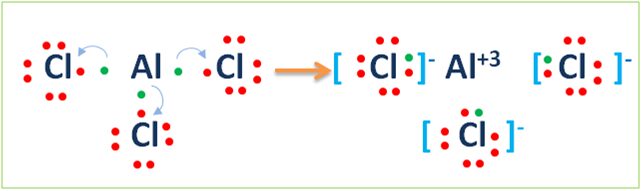
Aşağıdaki gösterim de yanlış değildir.Bazen böyle de gösterilebilir.

Al atomu 1.e- nu verir Al+1 olur
Al atomu 2.e- nu verir Al+2 olur
Al atomu 3.e- nu verir Al+3 olur
Cl atomları 1 e alırlar -1 yüklü olurlar
Kovalent Bileşiklerin Adlandırılması Konu Anlatımı Videosu TIKLA İzle Kimya Denizi YOUTUBE

İyonik Bileşiklerin Adlandırılması Örnekler KİMYA DENİZİ Youtube TIKLA İzle
 İyonik Bileşiklerin Oluşumu Çaprazlanması Suda Çözünmesi Videolu Anlatım Tıkla İzle Kimya Denizi YOUTUBE
İyonik Bileşiklerin Oluşumu Çaprazlanması Suda Çözünmesi Videolu Anlatım Tıkla İzle Kimya Denizi YOUTUBE

