KOVALENT BAĞ Konu Anlatımı Apolar Polar Kovalent Bağ Örnekleri Lewis 9.Sınıf
KOVALENT BAĞ Nedir? Kovalent Bağ Türleri
Ametallerin kendi aralarında elektron ortaklığı ile oluşturdukları bağlara Kovalent Bağ denir..Ametaller kendileri gibi ametal olan atomlarla bağ yapabilmek için elektron ortaklığı ile bağ oluştururlar.Elekron ortaklığı ile oluşan bu bağlar KOVALENT BAĞLAR olarak adlandırılır.
H2, O2, Cl2, H2O, HF, CH4, SO2 gibi yapılar kovalent bağla oluşan yapılardır.
Genel olarak 2 türlü Kovalent Bağ bulunur:
1.Apolar Kovalent Bağlar
2.Polar Kovalent Bağlar
Detaylı olarak inceleyelim;
1.APOLAR KOVALENT BAĞLAR KONU ANLATIMI ÇÖZÜMLÜ ÖRNEKLER
Aynı tür ametaller arasında elektron ortaklığı ile oluşan bağlar Apolar Kovalent Bağlar olarak adlandırılır. H2,O2,Cl2Br2 , O3 gibi aynı ametalden oluşmuş yapılar Apolar Kovalent Bağla oluşan yapılardır.
Apolar Kovalent Bağlar Örnekler apolar kovalent bağ örnekleri
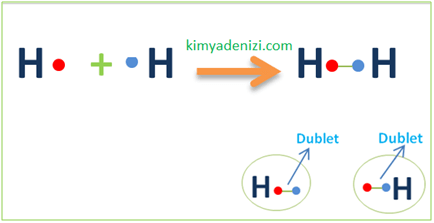
Örnek: H2 Molekülü Lewis Yapısı Simgesi Apolar Kovalent Bağ Oluşumu(1H)
1H :1Des( Değerlik e- sayısı):1 1 nokta 1bağ
Soygaz düzenine ulaşmak için(En yakın sogaz2He) 1 bağ yapar
H2 Molekülünde 2 H olduğu için 2 tane H alırız.
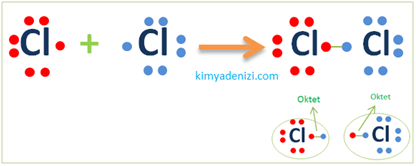
Örnek: Cl2 Molekülü Lewis Yapısı Simgesi Apolar Kovalent Bağ Oluşumu(17Cl)
17Cl :2.8.7 Des1 1 nokta 1bağ
Soygaz düzenine ulaşmak için(2.8.8) 1 bağ yapar
Cl2 Molekülünde 2 Cl olduğu için 2 tane Cl alırız.
 9.SINIF KİMYA KAZANIM TESTLERİ ÇÖZÜMLERİ İÇİN TIKLA
9.SINIF KİMYA KAZANIM TESTLERİ ÇÖZÜMLERİ İÇİN TIKLA
Örnek: F2 Molekülü Lewis Yapısı Simgesi Apolar Kovalent Bağ Oluşumu(9F)
9F :2.7 Des1 1 nokta 1bağ
Soygaz düzenine ulaşmak için(2.8) 1 bağ yapar
F2 Molekülünde 2 F olduğu için 2 tane F alırız.

Örnek:Br2 Molekülü Lewis Yapısı Simgesi Apolar Kovalent Bağ Oluşumu(35Br)
35Br :2.8.18.7 Des77 nokta 1bağ
Soygaz düzenine ulaşmak için(2.8.18.8) 1 bağ yapar
Br2 Molekülünde 2 Br olduğu için 2 tane Br alırız.

İKİLİ BAĞLAR ÜÇLÜ BAĞLAR TANIMI YAPISI OLUŞUMU
İki atom kendi arasında bağ yaparken ;
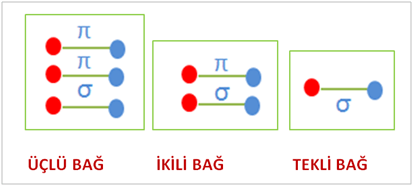
1 tane bağ yaparsa TEKLİ BAĞ
2 tane bağ yaparsa İKİLİ(ÇİFT) BAĞ
3 tane bağ yaparsa ÜÇLÜ BAĞ olarak adlandırılır.
O2 molekülünde ikil bağ, N2 molekülünde üçlü bağ oluşur.
İlk oluşan en alttaki bağ sigma bağı(σ) olarak adlandırılır
Üstünde oluşan 2.ve 3. Bağ lar ise pi π bağlarıdır
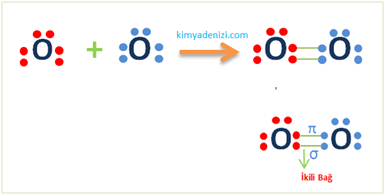
Örnek:O2 Molekülü Lewis Yapısı Simgesi Apolar Kovalent Bağ Oluşumu(8O)
8O :2.6 Des66 nokta 2bağ
Soygaz düzenine ulaşmak için(2.8) 2 bağ yapar
O2 Molekülünde 2 O olduğu için 2 tane O alırız.
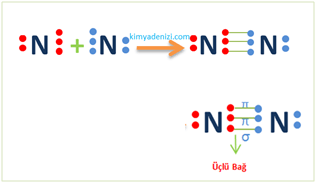
Örnek:N2 Molekülü Lewis Yapısı Simgesi Apolar Kovalent Bağ Oluşumu(7N)
7N :2.5 Des55 nokta 3bağ
Soygaz düzenine ulaşmak için(2.8) 3 bağ yapar
N2 Molekülünde 2 N olduğu için 2 tane N alırız.
2.POLAR KOVALENT BAĞLAR KONU ANLATIMI ÇÖZÜMLÜ ÖRNEKLER polar kovalent bağ örnekleri
Farklı tür ametaller arasında elektron ortaklığı ile oluşan bağlar Polar Kovalent Bağlar olarak adlandırılır. H2O,SO2,HCl2HBr ,CO2 , CS2 , gibi aynı ametalden oluşmuş yapılar Polar Kovalent Bağla oluşan yapılardır.
Örnek: HCl Molekülü Lewis Yapısı Simgesi polar Kovalent Bağ Oluşumu(1H, 17Cl)
1H :1Des(Değerlik e- sayısı):1 1 nokta 1bağ
17Cl :2.8.7 Des1 1 nokta 1bağ

Örnek: HF Molekülü Lewis Yapısı Simgesi Polar Kovalent Bağ Oluşumu(1H, 9F)
1H :1Des(Değerlik e- sayısı):1 1 nokta 1bağ
9F :2.7 Des1 1 nokta 1bağ

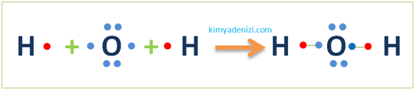
Örnek: H2O Molekülü Lewis Yapısı Simgesi Apolar Kovalent Bağ Oluşumu(1H, 8O)
1H :1Des(Değerlik e- sayısı):1 1 nokta 1bağ
8O :2.6 Des 6 6 nokta 2bağ MERKEZ ATOM O (Daha çok bağ yaptığı için)
Soygaz düzenine ulaşmak için(2.8) 2 bağ yapar
H2O Molekülünde 1H ve 2 O olduğu için 1 tane H 2 tane O alırız.
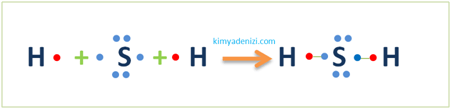
Örnek: H2S Molekülü Lewis Yapısı Simgesi PolarKovalent Bağ Oluşumu(1H, 16S)
1H :1Des (Değerlik e- sayısı):1 1 nokta 1bağ
16S :2.8.6 Des66 nokta 2bağ MERKEZ ATOM S (Daha çok bağ yaptığı için)
Soygaz düzenine ulaşmak için(2.8.8 ) 2 bağ yapar
H2S Molekülünde 1H ve 2 S olduğu için 1 tane H 2 tane S alırız.
Örnek: OF2 MolekülüLewis Yapısı Simgesi PolarKovalent Bağ Oluşumu(1H, 8O)
9F :2.7 Des:7 7 nokta 1bağ
8O :2.6 Des66 nokta 2bağ MERKEZ ATOM O (Daha çok bağ yaptığı için)
Soygaz düzenine ulaşmak için(2.8) 2 bağ yapar
OF2 Molekülünde 1O ve 2 F olduğu için 1 tane O 2 tane F alırız.

Örnek: CO2 Molekülü Lewis Yapısı Simgesi PolarKovalent Bağ Oluşumu(8O)
8O :2.6 Des66 nokta 2bağ
Soygaz düzenine ulaşmak için(2.8) 2 bağ yapar
6C :2.4 Des44 nokta 4bağ
Soygaz düzenine ulaşmak için(2.8) 4 bağ yapar
Merkez atom ortaya alınacak atomdur.Çok bağ yapan atom veya atomlar merkez atomlardır.Burada C daha çok bağ yaptığı için merkez atomdur.
CO2 Molekülünde 2 O olduğu için 2 tane O,1 tane C atomu alırız.

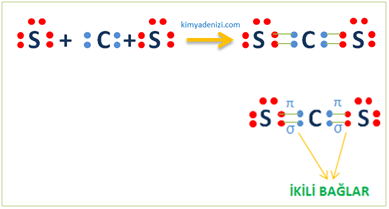
Örnek: CS2 Molekülü Lewis Yapısı Simgesi PolarKovalent Bağ Oluşumu(8O,6C )
16S :2.8.6 Des6 6 nokta 2bağ
Soygaz düzenine ulaşmak için(2.8.8 ) 2 bağ yapar
6C :2.4 Des4 4 nokta 4bağ
Soygaz düzenine ulaşmak için(2.8) 4 bağ yapar
Merkez atom ortaya alınacak atomdur.Çok bağ yapan atom veya atomlar merkez atomlardır.Burada C daha çok bağ yaptığı için merkez atomdur.
CS2 Molekülünde 2 S olduğu için 2 tane S,1 tane C atomu alırız.
Kovalent Bileşiklerin Adlandırılması Konu Anlatımı Videosu TIKLA İzle Kimya Denizi YOUTUBE

İyonik Bileşiklerin Adlandırılması Örnekler KİMYA DENİZİ Youtube TIKLA İzle
 İyonik Bileşiklerin Oluşumu Çaprazlanması Suda Çözünmesi Videolu Anlatım Tıkla İzle Kimya Denizi YOUTUBE
İyonik Bileşiklerin Oluşumu Çaprazlanması Suda Çözünmesi Videolu Anlatım Tıkla İzle Kimya Denizi YOUTUBE

